EGFLAM : découverte d'un nouveau gène lié à la cécité nocturne stationnaire congénitale complète
L'équipe dirigée par Isabelle Audo et Christina Zeitz à l'Institut de la Vision, en collaboration avec des cliniciens des Pays-Bas*, a identifié des mutations dans un nouveau gène responsables d'un trouble oculaire rare appelé cécité nocturne stationnaire congénitale complète. Cette découverte, publiée début décembre 2025 dans la revue JAMA Ophthalmology*, ouvre la voie à de meilleurs diagnostics et approfondit notre connaissance des pathologies oculaires en général. Le gène en question, appelé EGFLAM, en plus d'être lié à ce trouble rétinien héréditaire, explique et confirme certains mécanismes du développement de la myopie.
La CSNB, une maladie rare avec des cas génétiquement non résolus
La cécité nocturne stationnaire congénitale (CSNB) est une maladie génétique rare de la rétine, présente dès la naissance, qui empêche les yeux de bien voir dans le noir. Les patients voient peu ou pas la nuit, et présentent souvent un risque élevé de myopie en plus d'autres symptômes oculaires. Parmi les cas connus de CSNB, des chercheurs de l'Institut de la Vision et leurs collaborateurs ont déjà identifié 20 gènes impliqués dans différentes formes de CSNB, dont 5 conduisant à une cécité nocturne congénitale stationnaire complète (cCSNB) systématiquement associée à une myopie forte. Cette dernière éclipse souvent le diagnostic de la cCNSB, qui nécessite des examens cliniques spécifiques pour être correctement diagnostiquée. De plus, l'origine génétique de certains patients atteints de cCSNB reste inconnue. L'existence de ces cas « non résolus » implique un diagnostic et une prise en charge moins précis des patients. C'est pourquoi, dans le cadre du programme européen MyoTreat, l'équipe de Christina Zeitz et sa doctorante Sanja Boranisajevic, ont pour mission d'étudier le génome des patients non résolus atteints de CSNB associée à une myopie forte, afin de mieux comprendre les mécanismes conduisant à la myopie dans ces maladies.
Une découverte issue d'une collaboration clinique européenne
À l'origine de cette étude, deux patients de famille française d'origine marocaine ont été évalués par le Dr Vasily Smirnov et diagnostiqués comme atteints de cCSNB dans deux centres de référence en France**. Ils y sont suivis depuis l'enfance et ont subi des examens ophtalmologiques approfondis par des spécialistes des maladies rétiniennes héréditaires. Les auteurs de l’étude ont réalisé des analyses pour révéler la cause génétique de leur maladie. Ils ont d’abord vérifié la présence de mutations dans des gènes connus pour être impliqués dans les maladies rétiniennes héréditaires. En l'absence de résultats, ils ont opté pour des méthodes de séquençage plus larges à l'échelle du génome, fournissant des informations sur différents gènes potentiellement associés à la maladie. En utilisant des outils bioinformatiques, l'équipe de l'Institut de la Vision a réduit la liste des variants potentiellement implqués. En croissant leurs données avec la literature scientifique, ils ont prédit qu'un variant trouvé dans le gène EGFLAM serait à l'origine de la maladie. Les chercheurs l’ont ensuite confirmé chez les patients et certains membres de leur famille. Parallèlement, leurs collaborateurs du Centre médical universitaire de Radboud et de l'hôpital ophtalmologique de Rotterdam aux Pays-Bas ont identifié un autre cas de cCSNB non résolu, portant une mutation différente dans le même, gène confirmant la découverte.
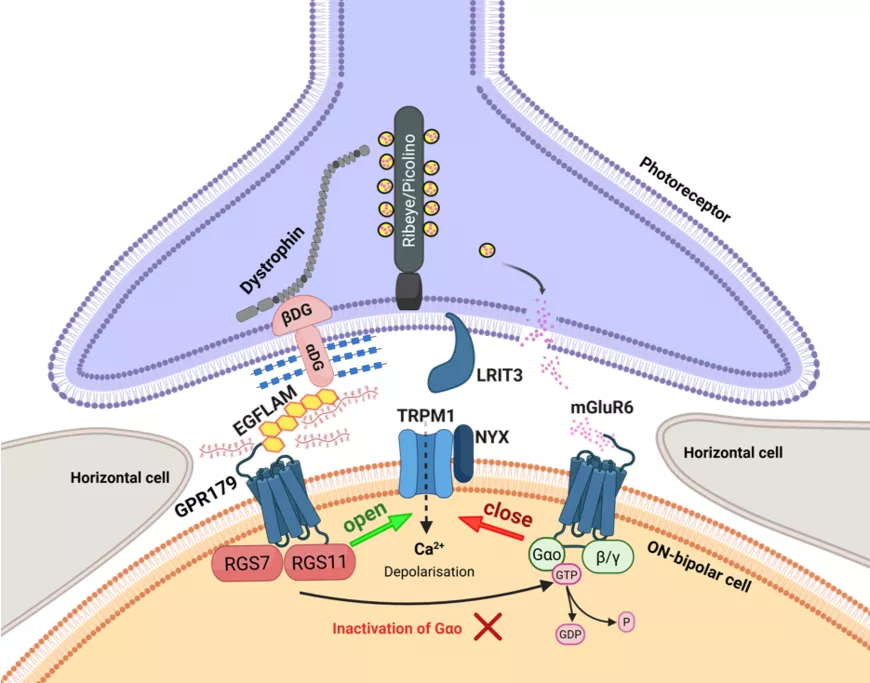
La mutation du gene EGFLAM perturbe la voie de signalisation ON au sein des cellules bipolaires de la rétine, importante pour la signalisation rétinienne. Cette voie est essentielle pour percevoir les contrastes lumineux sur les fonds sombres, dont l'absence conduit à la cécité nocturne et à une forte myopie observée chez cCSNB.
Une étape importante pour la recherche et les patients
Grâce au travail des chercheurs, EGFLAM rejoint la liste des 5 gènes à surveiller pour le diagnostic de cCSNB, probablement l'un des derniers compte tenu de la rareté des variants. Pour les familles concernées, avoir un nom et une cause génétique précise permet enfin un conseil adapté et une meilleure surveillance ophtalmologique. La découverte d’EGLFAM va également permettre de mieux comprendre les voies moléculaires impliquées dans la myopie, couramment observée chez les patients atteints de CSNB. L'étude des interactions entre cette protéine et d'autres impliquées dans la voie de signalisation ON dans la rétine pourrait fournir de nouvelles stratégies thérapeutiques pour la myopie, qui est l'objectif ultime du programme MyoTreat.
Lisez l'article complet : https://jamanetwork.com/journals/jamaophthalmology/fullarticle/2842379
* Boranijasevic S*, Smirnov V*, Navarro J, et al. Variantes pathogènes de l'EGFLAM et cécité nocturne stationnaire congénitale. JAMA Ophthalmol. Publié en ligne le 4 décembre 2025. doi :10.1001/jamaophthalmol.2025.4888
**Centre national de référence pour les maladies rétiniennes rares, hôpital Quinze-Vingts, Paris ; Centre de référence pour les maladies oculaires rares, l'exploration de la vision et la neuro-ophtalmologie, Hôpital universitaire de Lille
