Des organoïdes rétiniens pour prédire l’efficacité des thérapies géniques
Les chercheurs de l’Institut de la Vision ont évalué l’efficacité de l’édition génomique par CRISPR-Cas9 sur les organoïdes rétiniens par rapport aux modèles couramment utilisés pour développer des thérapies géniques. Leur publication*, parue en décembre 2025 dans le journal Molecular Therapy Methods & Clinical Development, montre que ces structures 3D cultivées en laboratoire reproduisent fidèlement les résultats obtenus in vivo, ouvrant la voie à des thérapies géniques plus sûres et plus efficaces pour les maladies rétiniennes héréditaires.
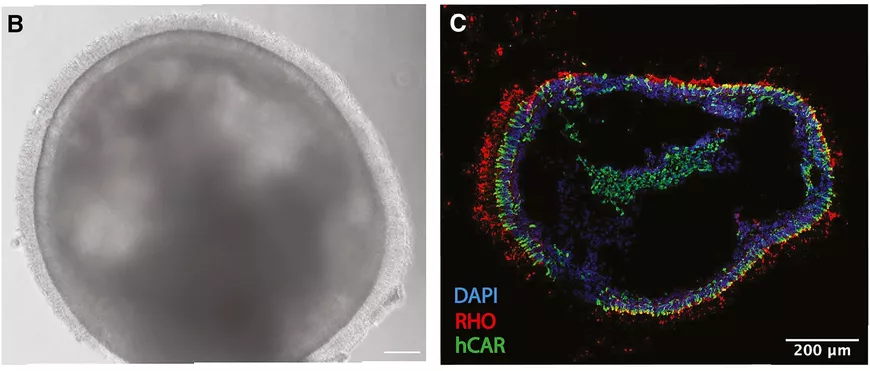
(B) Organoïde rétinien de 150 jours, la présence de cils à sa surface indique la présence de photorécepteurs. (C) Cryosection d’un organoïde rétinien. En rouge la rhodopsine, indicatrice de la présence de bâtonnets ; en vert l’arrestine, indicatrice de la présence de cônes.
Le défi des thérapies géniques pour la rétine
Les rétinopathies pigmentaires sont des maladies héréditaires causées par des mutations dans plus de 90 gènes différents, entraînant le dysfonctionnement ou la mort des photorécepteurs. Pour restaurer la vision chez les patients atteints, la piste la plus prometteuse est celle de la thérapie génique, qui vise à corriger ou compenser le gène défectueux. Si des succès ont été atteints, la diversité et la complexité des rétinopathies pigmentaires rendent les approches globales difficiles. Les thérapies utilisant des outils d’édition génomique, tels que les ciseaux moléculaires CRISPR-Cas9, pourraient offrir des solutions thérapeutiques personnalisées, adaptées à chaque mutation. Cependant, les modèles expérimentaux classiques ne permettent pas de reproduire fidèlement l’environnement génomique et structurel des photorécepteurs humains malades. Cette absence de modèle approprié rend incertain le passage en clinique des thérapies potentielles : il est difficile de prévoir avec précision leur efficacité chez l’humain.
De la cellule à la rétine : les organoïdes passent le test
Pour accélérer la recherche, l’équipe Thérapie géniques et modèles des maladies neurodégénératives, dirigée par Deniz Dalkara à l’Institut de la Vision, mise sur un modèle expérimental en plein essor : les organoïdes rétiniens. Ces minuscules structures biologiques en trois dimensions, d’à peine quelques millimètres, sont beaucoup plus proches de ce qui se passe dans notre organisme que les cultures cellulaires classiques en deux dimensions. Même s’ils ne reproduisent pas exactement un organe, les organoïdes offrent un accès beaucoup plus approfondi aux processus biologiques et à leurs dérèglements pathologiques. Il est même possible de créer des organoïdes à partir de cellules de patients, par exemple en prélevant des cellules de leur peau pour les reprogrammer en cellules souches induites (iPS). Cette méthode reproduit fidèlement l’environnement génomique et physiologique spécifique d’un patient – avec ses mutations – particulièrement précieux dans le cadre du développement de thérapies géniques contre les rétinopathies pigmentaires.
Afin d’explorer le potentiel des organoïdes rétiniens dans ce contexte, Juliette Pulman et Hugo Malki, chercheurs au sein de l’équipe de Deniz Dalkara, ont comparé leur réponse à l’édition génomique par CRISPR-Cas9 aux modèles classiques.
Pour leur étude, ils ont utilisé des organoïdes rétiniens âgés de 150 jours, issus des cellules de peau d’un donneur sain. La maturité avancée de ces organoïdes leur permet de développer des structures naturellement présentes dans la rétine, notamment des photorécepteurs fonctionnels dont le segment externe capte la lumière. Les chercheurs ont également utilisé une lignée cellulaire humaine couramment utilisée dans les études sur les thérapies géniques, ainsi qu’un modèle in vivo porteur de mutations du gène RHO. Ce gène, impliqué dans une forme de rétinopathie pigmentaire pour laquelle il n’existe pas de traitement, code pour un pigment visuel présent dans les photorécepteurs, la rhodopsine. C’est la cible qui a été choisie pour cette expérience.
Pour amener la modification génétique jusqu’au gène RHO, deux stratégies de livraison ont été testées. La première est un système de double vecteur viral AAV contenant CRISPR-Cas9, couramment utilisé en thérapie génique. La deuxième est un complexe moléculaire RNP contenant seulement la protéine Cas9, plus difficile à mettre en œuvre mais moins inflammatoire.
Avec ces deux stratégies, les chercheurs ont observé dans les organoïdes des taux d’édition génomique bien plus faibles que ceux observés dans les lignées cellulaires en 2D mais cohérent avec les modèles in vivo. Leurs résultats montrent que dans les organoïdes rétiniens, les segments externes des photorécepteurs agissent comme une barrière physique, limitant l’entrée des outils d’édition génomique dans le noyau. Ce phénomène est comparable à celui observé dans les rétines vivantes.
Vers une accélération de la recherche translationnelle
En montrant que les organoïdes "reproduisent" les résultats in vivo, l'étude valide l'utilisation de ces « avatars de rétine » pour servir de pont entre la recherche fondamentale et la clinique. Les résultats suggèrent que la réussite d’une thérapie génique sur des organoïdes serait représentative de sa réussite chez l’humain, permettant d’optimiser les traitements, de minimiser le recours aux modèles animaux et d’accélérer le développement de thérapies géniques personnalisées. À terme, l’utilisation des organoïdes pourrait révolutionner le traitement des maladies héréditaires de la rétine, en rendant les thérapies plus sûres, plus efficaces et plus accessibles aux patients. C’est dans ce but que l’Institut de la Vision, pionnier des organoïdes rétiniens à travers plusieurs protocoles brevetés, agrandit son laboratoire de culture.
Découvrez en vidéo le parcours de Juliette Pulman, première autrice de l’étude : https://www.linkedin.com/feed/update/urn:li:activity:7427380974075691008
* Juliette Pulman, Hugo Malki, Paul Oudin, Ecem Aydin, Sophie Tran, Laura Visticot, Camille Robert, Anne De Cian, Marie As, Olivier Goureau, Jean-Paul Concordet, Deniz Dalkara, Retinal organoids mirror CRISPR-Cas9 gene editing efficiency observed in vivo, Molecular Therapy Methods & Clinical Development, Volume 33, Issue 4, 2025, 101627, ISSN 2329-0501.
Lien vers l’étude : https://www.cell.com/molecular-therapy-family/advances/fulltext/S2329-0501(25)00222-0
